מה חשוב לדעת בקשר ליוד ובלוטת התריס
- יעל שחם-גפני
- 29 במאי 2021
- זמן קריאה 20 דקות
עודכן: 30 במאי 2021

יוד הוא נושא שנוי במחלוקת בהקשר של בריאות בכלל ותפקוד בלוטת התריס בפרט.
מחסור ביוד גורם למגוון של בעיות בריאות שהידועה בהן היא זַפֶּקֶת (Goiter) – בלוטת תריס מוגדלת שמופיעה כהתנפחות של החלק הקדמי של הצוואר. עוד נושא חשוב מאוד שיוד משפיע עליו הוא התפתחות העובר, ומחסור ביוד עלול להשפיע לרעה על התפתחות העובר והתינוק ובמקרים חמורים לגרום לקרטיניזם - פיגור שכלי ופיגור בגדילה. כמו כן נמצא קשר בין מחסור ביוד וסיכון מוגבר לחלות בסרטן השד.
מכיוון שמחסור ביוד גורם לבעיות בהתפתחות העובר ועלול להשפיע על רמת האינטלגנציה של אוכלוסיה, מדענים חקרו מהי הרמה המינימלית הדרושה כדי למנוע את התופעה הזו. על סמך מחקרים אלה המועצה האמריקאית למזון ותזונה קבעה את הכמות המומלצת ליוד, ה- RDA, לרמה של 150 µg (מיקרוגרם).
בהתיחס למדד זה, בתחילת שנות ה 90 האוכלוסיה באזורים נרחבים של העולם סבלה ממחסור ביוד, ועל כן ב- 1993 ארגון הבריאות העולמי הוציא את הדוח הראשון שלו [1] בנושא מחסור ביוד ובהמשך מדינות שונות החלו בתוכניות לאומיות למיגור המחסור ביוד, במסגרתן בוצעה העשרה של מלח שולחן ביוד. במקביל ליישום של תוכניות אלה חלה עלייה בהיארעות של מחלות אוטואימוניות של בלוטת התריס: השימוטו וגרייבס.
כיום הדעה הרווחת בקרב רופאים קונבנציונאליים ואנדוקרינולוגים היא שיוד בכמויות גדולות מידי יכול להזיק. איזבלה וונץ, רוקחת ומומחית בנושא השימוטו כותבת בבלוג באתר שלה:
בעולם הרוקחות אִמְרָה ידועה היא ש"ההבדל בין תרופה ורעל זה המינון". זו אמירה של המדען פאראצלסוס שחי במאה ה 15, אשר נחשב לאחד ממייסדי הרפואה המודרנית ואבי הטוקסיקולוגיה.
ארגון הבריאות העולמי הגדיר מדד להעריך את המצב של יוד בקרב אוכלוסיה [2]. מדד זה בוחן את כמות היוד המופרשת בשתן, ולוקחת את החציון של קבוצת הנבדקים. בדו"ח של הארגון מופיעה הטבלה הבאה:
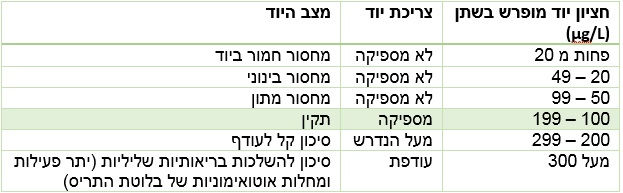
חשוב להבין את המספרים האלה. אם הכמות המומלצת לצריכה היא 150 מיקרוגרם, וברמת צריכה מספיקה אדם מפריש בין 100 ל 199 מיקרוגרם לליטר, וכמות השתן שאדם בריא מפריש ביום היא 1.5 ליטר, זה אומר שהוא יפריש בין 150 ל 298 מיקרוגרם ליום, משמע הכמות המופרשת היא מעל הכמות שמומלץ לצרוך. כלומר יש סתירה בין ההמלצה של ה RDA וההגדרות של ארגון הבריאות העולמי.
מהצד השני של המתרס ישנה קבוצה של רופאים כמו דר אברהם, דר פלצאס, דר האקלה, ודר ברוונשטיין שאומרים שה RDA נמוך מידי, אינו מספיק לתמוך בבריאות אופטימלית, ולמרות התוכניות למיגור המחסור ביוד, עדיין רוב האוכלוסיה במדינות המערביות סובלת מחוסר ביוד, אשר הינו גורם מרכזי במחלות של בלוטת התריס וסרטן השד.
במאמר זה אביא את טיעוניהם של שני הצדדים כדי שתוכלו להגיע להחלטה מושכלת בעצמכם. אבל לפני שנתעמק בסוגיה חשוב להבין כיצד בלוטת התריס עושה שימוש ביוד כדי לייצר את ההורמון שלה T4.
מה אנחנו יודעים על יוד ואיך בלוטת התריס עושה בו שימוש
יוד הוא יְסוֹד קֹרֶט (יסוד כימי הדרוש לגוף במינונים פיצפונים) ויש לו תפקיד חשוב בתהליכים בגוף. רוב היוד, בין 70-80%, נמצא בבלוטת התריס שמשתמשת בו לייצר את ההורמונים שלה. ליוד תפקיד חשוב בהתפתחות העובר והילד, לכן יוד נמצא גם ברקמת השד ובחלב של נשים מיניקות. יוד נמצא גם ברקמות בעין, בקיבה, בבלוטות הרוק ובצואר הרחם. התפקיד של יוד ברקמות הללו עדיין לא מובן דיו ע"י המדע. [3]
נתחיל עם קצת חומר רקע על איך בלוטת התריס מייצרת את ההורמון T4 בתוך התאים שלה. [4] התהליך מתחיל עם יוד שמסתובב בזרם הדם ומגיע לבלוטת התריס. חשוב לדייק כאן כי יש היוד מופע בשני אופנים בגוף:
האטום יוד שמסומן באות I ובאנגלית נקרא iodine
יון של יוד – אטום של יוד שיש לו עודף אלקטרון ומסומן ב I- ובאנגלית נקרא iodide
היוד אינו מפעפע לתוך התאים של בלוטת התריס. דרוש מנגנון מיוחד שמבוסס על הפרשי מתח חשמלי כדי להכניס את היוד לתאים, ולכן מה שנכנס לתאים אלה יונים של יוד. הורמון ה TSH הוא שמתניע את תהליך כניסת היונים הללו לתאים בבלוטה.
בשלב הבא נדרש לְחָמְצֵן את היונים של יוד לאטומים של יוד וזה נעשה בעזרת האנזים TPO ומימן על חמצני H2O2 (מי חמצן). היוד שכבר עבר את ההמרה יכול עכשיו להיקשר לחלבון תירוגלובולין Tg ולהמשך ייצור ההורמון. החימצון של היונים של יוד הוא תהליך שיכול לגרום להרבה מאוד נזק חימצוני לתא ולכן נדרשת לתא אספקה קבועה ורבה של נוגדי חימצון. נוגד החימצון העיקרי הוא החלבון גלותתיון. כדי לייצר את החלבון הזה תאי הבלוטה זקוקים למינרל סלניום ולויטמינים הדרושים לתהליך המתילציה: B6, B9, B12 וביוטין. כאשר יש יוד בשפע נוצרות גם חומצות שומן מיודדות שנקראות דלתא-איודו-לקטון. החומרים האלה מווסתים את חימצון היוד ובכך תורמים למניעה של נזק חימצוני בבלוטה.
הכנתי סרטון אנימציה קצר שממחיש את התהליך:
טענות המצדדים בהגבלה של יוד לחולים במחלות של בלוטת התריס
בעבר, מחסור ביוד היה נושא לדאגה כלל עולמית. אפילו עד שנות ה 90 רק באחוז קטן של המדינות אנשים קיבלו מספיק יוד, ו 112 מדינות היו מוגדרות ע"י ארגון הבריאות העולמי כבעלות "מחסור חמור ביוד".
כדי לטפל בבעיה, ארגוני בריאות עולמיים התאחדו והתחילו להעשיר מלח ומזונות אחרים ביוד, והמצב במדינות העולם השתנה במשך שני עשורים. עד 2014 לא היו יותר מדינות בהן יש מחסור ביוד לתושבים. זו נחשבה להצלחה גדולה.
עם זאת, העלייה החדה בצריכה של יוד בעולם במשך שני העשורים האחרונים, עוקבת אחר העלייה מרקיעת השחקים במחלות של בלוטת התריס כמו תת פעילות, השימוטו, וסרטן בבלוטת התריס. בעוד קורלציה אינה בהכרח מעידה על סיבתיות, המחקר מאשש את התיאוריה שעודף יוד עלול להוביל לפגיעה בפעילות של בלוטת התריס.
מחקרים על מלח מועשר ביוד ובריאות בלוטת התריס
באפריל 2021 פורסם מאמר סקר [5] שבוחן את הקשר בין תוכנית התיסוף של יוד ומצב המחלות האוטואימוניות בבלוטת התריס. במאמר החוקרים דנים בשאלה האם התוכנית העולמית להעשרת מלח ביוד השפיעה על העליה במחלות אוטואימוניות של בלוטת התריס.
לדברי החוקרים:
האפידמולוגיה של מחלות של בלוטת התריס עברה שינוי משמעותי מאז הפעלת התוכניות להעשרת מלח ביוד, ובאופן ספציפי התוצאה שנצפתה היא הפחתת השכיחות של גויטר, הפחתת השכיות של תת פעילות אצל תינוקות, שיפור התפקוד הקוגנטיבי וההתפתחות של תינוקות, והיארעות מופחתת של הסוגים האגרסיביים של סרטן בלוטת התריס.
לגבי ההשפעה על מחלות אוטואימוניות של בלוטת התריס, בניסויים על מודל מהונדס של עכברים שנוטים לפתח מחלה אוטואימונית בבלוטת התריס נמצא שיוד עלול לגרום או להגביר אוטואימוניות בבלוטת התריס, אבל עדיין לא ברור אם השינויים שחלו במערכת החיסון הם בגלל השפעה ישירה של היוד על התגובה החיסונית או שזו תופעה עקיפה שהיא תגובה לנזק שיוד גורם לתאי הבלוטה.
רמת היוד בקרב האוכלוסיה לפני הפעלת תוכנית ההעשרה כנראה משפיעה על התגובה של הבלוטה ועל ההתפתחות של מחלות אוטואימוניות. יתר על כן, ההימצאות של נוגדני בלוטת התריס, שנחשבת כסממן מובהק של מחלה אוטואימונית של הבלוטה, משתנה בין אוכלוסיות תחת ההשפעה של גורמים גנטיים וסביבתיים, והנוכחות של נוגדני בלוטת התריס אינה תמיד חופפת להימצאות של מחלה בבלוטה או התפתחות עתידית של מחלה כזו. בנוסף, יש מגמה כללית של עלייה בהיארעות של מחלות אוטואימוניות בעשורים האחרונים.
המסקנה שלנו היא שצריכה יתרה של יוד בשל תוכנית העשרה ללא בקרה מספקת עלולה לגרום לבעיות בתפקוד של בלוטת התריס כולל מחלה אוטואימונית, אשר באה לידי ביטוי לרוב בתת פעילות סאב קלינית אוטואימונית. על כן יש לבקר באופן הדוק את תוכניות ההעשרה ולדאוג למנוע גם מחסור ביוד, וגם עודף.
להלן תוצאות של מספר מחקרים שנעשו בעקבות התוכנית העולמית להעשרת מלח שולחן ביוד. מחקרים כאלה נעשו בסין [6], בהודו [7], במדינות שונות באירופה [8], ובמדינות נוספות. בישראל לא הופעלה תוכנית להעשרת מלח ביוד, רק לאחרונה [9] (2017) בחנו את מצב היוד ונמצא שהאוכלוסיה סובלת ממחסור ביוד.
רוב המחקרים מדווחים על המגמות הבאות:
ירידה באחוז התושבים שסובלים מהגדלה של בלוטת התריס (גויטר)
עליה זמנית של יתר פעילות של הבלוטה שירדה לאחר זמן וחזרה לרמה המקורית
עליה של השכיחות של מחלה אוטואימונית בבלוטת התריס.
מירב המחקרים לא התיחסו ספציפית למדדים של נוגדנים לבלוטת התריס, אולם כמה מחקרים כן בחנו את הסוגיה הזו:
חוקרים באיראן [10] מדדו את ההיארעות של זפקת והרמה של נוגדנים לאנזים תירואיד פרוקסידז (TPO) ולתירוגלובולין (Tg) לפני ואחרי התוכנית הלאומית להעשרת מלח ביוד. שהתחילה ב 1994. בשנים 1983-84, זפקת נמצאה ב 12.1% מהאוכלוסיה, ונוגדנים חיוביים נמצאו באוכלוסיה אצל 3.2% ל TPO, ו4% ל Tg, על פי מדגם של 465 מבוגרים תושבי טהרן. מדגם נוסף של 1426 תושבים מטהרן נערך בשנים 1999-2000, ואז נמצאה זפקת אצל 9.7%, 12.5% נמצאו חיוביים ל TPO ו 16.8% חיוביים ל Tg. המחקר מראה עלייה פי 4 ברמות הנוגדנים במשך 16 שנה, מתוכן 6 שנים בהן התקיימה תוכנית ההעשרה.
מחקר דומה בוצע באזור שריאר באיראן [11] שבו מחלת הזפקת היתה נפוצה. בשנת 1983 בה בוצע הסקר הראשון נמצאה זפקת אצל 60% מהנבדקים, וכמות היוד המופרשת היתה 7.6 מיקרוגרם לליטר (זוכרים, האופטימלי הוא בין 100 ל 200). לאחר 12 שנה של העשרת מלח ביוד נמצאה זפקת אצל 46% מהנבדקים, וכמות היוד המופרשת היתה 18.5 מיקרוגרם לליטר. המחקר הראה שחלה ירידה באחוז הסובלים מזפקת, חלה עלייה בכמות היוד המופרש בשתן, אך הוא עדיין הרבה מתחת לרמה התקינה שהוגדרה ע"י ארגון הבריאות העולמי. המחקר לא מצא שינוי ברמות הנוגדנים שנצפו אצל הנבדקים.
מחקר אחר מסלובניה [12] בחן את ההיארעות של מחלות של בלוטת התריס בקרב האוכלוסיה בסלובניה לאחר שהעלו את מינון היוד המועשר במלח שולחן מ 10 מג/קג ל 25 מג/קג בשנת 1999. התוצאה של העלאה זו היתה ירידה במקרים של זפקת לשישית ממה שהיה לפני הפעלת התוכנית, ומנגד עליה בהיארעות של השימוטו כמעט פי 2.
מחקר מאיטליה [13] בחן את הנוגדנים ל TPO ול Tg בקרב 906 משתמשי מלח מועשר ו 389 שהשתמשו במלח רגיל. מתוך אוכלוסיה זו בחנו את בלוטת התריס באולטראסאונד כדי לגלות חולי השימוטו ונמצאו 87 מקרים. בדיקת הנוגדנים בקרב החולים הראתה ל-Tg אצל משתמשי מלח מועשר 58.4% לעומת 31.8% אצל האחרים, ול 61.5%TPO לעומת 45.4%.
מחקרים בדבר מתן תוסף של יוד וחולי של בלוטת התריס
חוקרים בגרמניה [14] בחנו את ההשפעה של צריכה מוגברת של יוד על קבוצה של חולי זפקת שתפקודי בלוטת התריס שלהם היו תקינים. 62 נחקרים חולקו לשתי קבוצות. קבוצת הניסוי קיבלה מינון של 200 מיקרוגרם יוד וקבוצת הביקורת קיבלה פלסבו. משך הטיפול היה 12 חודשים, ומעקב ל 6 חודשים נוספים. אצל קבוצת הניסוי נצפתה ירידה של גודל בלוטת התריס ב 38% שנשמרה אחרי הפסקת הטיפול ביוד, בעוד שאצל קבוצת הביקורת לא היה שינוי. אצל שלושה אנשים מקבוצת הניסוי התפתחה דלקת בבלוטת התריס ונוגדנים לבלוטת התריס, שזה 10% מקבוצת הניסוי. מעקב לאורך שנתיים נוספות אחר משתתפי ניסוי אלה הראה שמצב הנוגדנים חזר לנורמה.
מחקר אחר מגרמניה [15] בחן את ההשפעה של תוסף יוד על אנשים בריאים, וטיפולים שונים לחולים בהשימוטו. מתוך קבוצה של 375 אנשים בריאים שליש קיבלו 200 מיקרוגרם יוד ליום, שליש קיבלו מנה שבועית של 1530 מיקרוגרם יוד, ושליש היוו קבוצת ביקורת. בקבוצת ה 200 מיקרוגרם ליום לא נצפה שינוי ברמות הנוגדנים ל TPO ול Tg. בקבוצת ה 1530 מיקרוגרם במנה שבועית נצפתה עלייה ברמות הנוגדנים הללו, פי 4 מאשר בשתי הקבוצות האחרות.
מתוך קבוצה של 377 חולים בהשימוטו חלק קיבלו טיפול תרופתי, חלק קיבלו שילוב של תרופה ומינון נמוך של יוד (בין 50 ל 150 מיקרוגרם ליום) וחלק קיבלו 200 מיקרוגרם ללא טיפול תרופתי. בקבוצות שקיבלו מנות נמוכות של יוד נצפתה ירידה ברמת נוגדני Tg ו TPO.
מה המכניזם שגורם לתגובה אוטואימונית בנוכחות צריכה מוגברת של יוד?
שמירה על הוֹמֵאוֹסְטָסִיס של הורמוני בלוטת התריס היא קריטית לבריאות, ולכן הגוף פיתח כל מיני מנגנונים להתמודד עם מחסור או עודף של יוד.
כאשר בלוטת התריס אצל אדם בריא נחשפת לכמויות גדולות של יוד קורית תופעה שמכונה אפקט וולף חייקוף: התהליך של היקשרות היוד לתירוגלובולין נבלם, ולכן גם ייצור ההורמונים מדוכא. האפקט נמשך כמה ימים ואז תהליך ייצור ההורמונים בבלוטה חוזר למצב התקין.
חשיפה לרמה גבוהה של יוד גורמת למות של תאים בבלוטת התריס [16]. אחת ההשערות לסיבה לכך היא הגברה של הנזק החימצוני שנגרם לתאים בשל חימצון היוד [17]. כאשר תאים מתים, חלק מהתוכן שלהם נשפך ומנוקז דרך נוזל הלימפה לבלוטת הלימפה הקרובה, שם כדוריות דם לבנות מעכלות את החומרים ומציגות אותם לתאים המייצרים נוגדנים. בנוסף, מגיעים לזירת הנזק תאים של מערכת החיסון כדי לסלק את התאים המתים. כל זה מתבטא בתהליך דלקתי בבלוטת התריס וייצור של נוגדנים – מצב אוטואימוני.
נמצא שמתן תוסף סלניום מיתן את התהליך החיסוני אצל עכברים שקיבלו תוסף יוד, כנראה בשל הפחתת הנזק החימצוני [18].
מחקר על ההשפעה של תזונה מפחיתת יוד
אם עודף של יוד עלול לגרום לנזק ותהליך דלקתי בבלוטת התריס, האם הגבלה של צריכת יוד יכולה להועיל?
בקוריאה חקרו בדיוק את השאלה הזו [19]. באזור בקוריאה שבו אנשים אוכלים הרבה מאכלי ים בחנו את ההשפעה של דיאטה מעוטת יוד בקרב מאובחני תת פעילות סאב קלינית (TSH גבוה אך T4 תקין). נבחרו משתתפים שהפרשת היוד בשתן אצלם היתה גבוהה (מעל 300 מיקרוגרם לליטר). אחרי תקופה של 3-6 חודשים של תפריט מופחת יוד שהביא לירידה של היוד המופרש לרמה שמתחת 300 מיקרוגרם לליטר רמת ה TSH ירדה בחצי (מ 9.0 ל 4.7) ורמת ה T4 עלתה (מ 1.11 ל 1.18).
ביפן [20] חוקרים בדקו את ההשפעה של תפריט המגביל את צריכת היוד על קבוצה בת 33 אנשים הסובלים מתת פעילות של בלוטת התריס (ללא דלקת בבלוטה למשך שנה לפחות). החולים הפחיתו את צריכת היוד למשך חודש עד חודשיים. לפני תחילת הטיפול רמת ה TSH היתה בממוצע 21.9 mU/L ולאחר צריכת תפריט מגביל יוד ירד ל 5.3 mU/L. 11 מהחולים הגיעו למצב של רמה תקינה (0.3-3.9 mU/L). לא נמצא קשר בין השיפור במדדי ה TSH למדדים של רמת הנוגדנים, אולם כן נמצא קשר עם תוצאה של בדיקת מיפוי הבלוטה עם (99m)Tc: השיפור ברמת ה TSH היה יותר גדול ככל שהיתה פחות קליטה של החומר הרדיואקטיבי בבלוטה. כמו כן נמצא קשר עם רמת היוד ההתחלתית: ככל שרמת היוד ההתחלתית היתה יותר גבוהה, השיפור ב TSH היה יותר גדול.
מחקר נוסף מקוריאה [21] בחן את ההשפעה של תפריט המגביל צריכת יוד למשך 3 חודשים על חולי השימוטו שלא קיבלו טיפול תרופתי. צריכת היוד היומית לפני תחילת הניסוי היתה גבוהה, הרבה מעל 300 מיקרוגרם, והפרשת היוד בשתן היתה מעל 300 מיקרוגרם לליטר בממוצע. בקבוצת הניסוי רמת ה TSH ההתחלתית היה בממוצע 37.95 IU/mL ובסוף הניסוי 25.66. רמת FT4 ההתחלתית היתה 0.8 ng/dL ובסוף הניסוי 0.98. התוצאות מראות שיפור של מדדי הבלוטה בקבוצת הניסוי. בקבוצת הביקורת רמת ה TSH ההתחלתית היה בממוצע 11.25 IU/mL ובסוף התקופה 14.27. רמת FT4 ההתחלתית היתה 0.98 ng/dL ובסוף התקופה 0.92. כלומר אצל קבוצת הביקורת חלה הרעה במדדי הבלוטה.
המסקנה משלושת המחקרים הללו היא שכאשר צריכת היוד היא גבוהה, הגבלת הצריכה של יוד עשויה להביא לשיפור במצב ההורמונים של בלוטת התריס.
סיכום טענות המצדדים בהגבלה של הצריכה של יוד לחולי השימוטו
מכל המחקרים האפידמולוגיים ומחקרי הניסוי מתקבל הרושם שאכן יש מינון אופטימלי של יוד. צריכה של פחות מידי יוד גורמת לעליה בחולים בזפקת, ואילו צריכה של יותר מידי יוד מעלה את המחלות הדלקתיות והאוטואימוניות בבלוטה. כמו כן, שינוי לא מבוקר של כמות היוד שאדם צורך כנראה יכולה להשפיע לרעה אצל אנשים הרגישים לכך. אצל אנשים שצורכים עודף של יוד ויש להם מחלה בבלוטת התריס, הפחתה של הצריכה עשויה להביא שיפור במדדים של תפקודי בלוטת התריס.
מצדדי היוד: עולם הרפואה לקה ביודופוביה
דר גיא אברהם יסד את פרויקט היוד בשנת 1998 כאשר גילה את היתרונות הבריאותיים הרבים של מתן תוסף יוד למטופליו. בהמשך הצטרפו אליו דר פלצאס, דר האקלה, ומאוחר יותר הצטרף אליהם דר ברוונשטיין שכתב את הספר Iodine: Why You Need It; Why You Can’t Live Without It.
בסדרה של שלושה מאמרים דר אבהרם מתעד את ההיסטוריה של היוד. המאמר הראשון [22] עוקב אחר יוד מהגילוי שלו בתחילת המאה ה-19, מציאת הקשר בין זמינות/מחסור של יוד בתזונה והתפתחות של גויטר באמצע המאה ה-19, הגילוי שבלוטת התריס מכילה הרבה יוד בסוף המאה ה-19, ועד הפיכתו לתרופת פלא לכל חולי. עד מלחמת העולם השנייה טיפול בתמיסת יוד בשם Lugol היתה מאוד נפוצה. הרופא הצרפתי ז'אן לוגול הציע אותה לשמוש בשנת 1829. התמיסה מכילה 5% יוד (אטומי) ו 10% אשלגן יודי (יונים של יוד) והמינון המומלץ היה שתי טיפות ליום שסיפקו 12.5 mg יוד.
יוד היה הטיפול המועדף ליתר פעילות של בלוטת התריס, ובשנת 1930 מאמר של תומפסון ושותפיו מתעד אחוז הצלחה של 88% עם תמיסת לוגול במינונים של 6-90 מ"ג.
יוד נמצא כיעיל לטיפול בגויטר. הרופאים שמו לב שבמדינות שבהן הקרקע ענייה ביוד, ילדים, ובעיקר ילדות, ביחס של 1:6, נוטים לפתח גויטר בגיל ההתבגרות. נעשו מספר מחקרים ונמצא שמתן תוסף יוד במינונים של 1.4 – 9 מ"ג יעיל למניעה וגם לטיפול בגויטר.
בעקבות הגילויים הללו הוצע להעשיר מלח ביוד. המינון היומי באופן צריכה זה נמוך בשני סדרי גודל מהמינון שהיה נהוג לתת בתמיסת לוגול, וכן הוא הכיל יוד בצורה של יונים ולא בצורתו האטומית. במקביל להוספה של יוד למלח החלו להופיע מקרים של מחלה אוטואימונית בבלוטת התריס. דר אברהם מדגיש שעד למועד זה, מחלות אוטואימוניות של בלוטת התריס לא היו מוכרות, למרות השימוש הנרחב בתוספים של יוד.
בניסויים בעכברים הצליחו לגרום למחלה אוטואימונית בבלוטה עם מינונים גבוהים של יוד רק כאשר הוסיפו תרופות גויטרוגניות. הגויטרוגנים גרמו להתרבות חריגה של תאים בבלוטה ולמחסור ביוד. נמצא שמתן של נוגדי חימצון מנע את ההתפתחות של התהליך האוטואימוני.
מכל המידע הזה דר אברהם מסיק שדוקא מינון נמוך ולא מספיק של יוד בתוספת של חומרים נוספים שהם גויטרוגניים (פוגעים בבלוטת התריס) הם הגורם למחלה האוטואימונית. המכניזם שדר אברהם משער כסיבה הוא פגיעה חימצונית בתאים בבלוטה. מחסור ביוד גורם ל TSH גבוה ורמה נמוכה של חומצות שומן מיודדות (דלתא-איודו-לקטון שדיברנו עליו בהתחלה). זה יחד עם הימצאות של עודף סידן (בגלל מחסור במגנזיום) גורמים להפעלת יתר של התהליך של חמצון היוד, דבר שגורם נזק חמצוני בתא ונזק חימצוני לאנזים TPO ולחלבון תירוגלובולין. הגוף מייצר נוגדנים כנגד החלבונים הפגועים הללו, ותאים לבנים מגיעים לאזור כדי לטפל בתאים שניזוקו.
דר אברהם טיפל בחולים ע"י מתן תוסף של יד במינון גבוה ותוסף מגנזיום ומצא את הטיפול יעיל למצבים אוטואימוניים בבלוטה.
במאמר השני [23] דר אברהם מתאר את ההסטוריה של גילוי ההורמונים של בלוטת התריס ועד השימוש בהורמונים סינטטיים לטיפול בתת פעילות.
במאמר השלישי [24] מתואר כיצד מסע יחסי הציבור לשימוש במלח מועשר ביוד והשימוש בתירוקסין כתרופה לתת פעילות דחקו את מקומו של יוד בצורה של תוסף, לטיפול במחלות של בלוטת התריס. בהמשך פורסם המאמר שהגדיר את אפקט וולף חייקוף בו הם מדווחים על מינון של יוד שעוצר את הקליטה של יוד ע"י בלוטת התריס. החוקרים הסיקו (באופן מוטעה כך טוען דר אברהם) שהפסקת הקליטה של יוד גורמת לתת פעילות וגויטר, אך לא מדדו את הפרמטרים הללו בניסויים שלהם. בהמשך פרסם וולף מאמר נוסף בו הוא מגדיר ארבע רמות של "עודף יוד". מכאן הדרך היתה סלולה למצב שהמחבר מכנה יודופוביה – הפחד מפני יוד.
מדוע נשים סובלות ממחלות של בלוטת התריס הרבה יותר מגברים?
דר אברהם הוא גניקולוג ואנדוקרינולוג בהתמחותו, ותמיד הוא תהה מדוע נשים נפגעות הרבה יותר ממחלות של בלוטת התריס, גם גויטר, גם תת פעילות, וגם מחלות על רקע אוטואימוני. הרבה נשים מפתחות את המחלה בגיל ההתבגרות, אחרות מאובחנות לאחר הריון ולידה.
התקופות האלה בחיי אישה הן תקופות בהן השדיים גדלות ומתפתחות, או מתכוננות להנקה. אחרי בלוטת התריס השד הוא האיבר שצורך הרבה יוד בגוף. האם יתכן שבתקופות שיש צריכת יוד מוגברת של השדיים, לא נשאר מספיק לבלוטת התריס ואז היא נפגעת?
מחקרים מראים שמחסור ביוד מעלה את הסיכון לחלות בסרטן השד [25]. מחקר שעקב אחר נשים שעוברות מומגרפיה מצא סיכון כפול לחלות בסרטן שד אצל נשים שנוטלות תרופות לבלוטת התריס: הסיכון הממוצע היה 6.2% לכלל האוכלוסיה ו 12.1% לנוטלות הורמוני בלוטת התריס. לאלה הנוטלות הורמונים יותר מ 15 שנה הסיכון עלה ל 19.5%.
כאמור למעלה, כמות היוד המומלצת שקבעה המועצה האמריקאית למזון ותזונה היא 150 µg, ו 1100 µg או 1.1 mg (מיליגרם) נקבעה לרמה המקסימלית שמעבר לה יתכן נזק. לעומת זאת, היפנים צורכים בין 1-3 mg לפי מחקר סקר שנעשה ב 2011 [26], הם מבין האנשים מאריכי החיים בעולם, ואחוזי סרטן השד הנמוכים בעולם.
האם נכון לקבוע את התצרוכת היומית הדרושה ליוד על פי הרמה המינימלית שבה לא מופיע גויטר? זה כמו שקבעו את הרמה הדרושה לויטמין C לזו שמונעת צפידיניה, אולם ברבות הימים התגלה שרמה זו נמוכה בסדרי גודל ממה שדרוש לפעולה אופטימלית של הגוף ומערכת החיסון בפרט.
מה אם כן רמת היוד הדרושה לגוף כולו?
במאמר משנת 2002 [27] כותבים דר אברהם ושותפיו:
"בשנת 1930 נכתב במאמר מאת תומפסון ושות': הכמות התקינה [של יוד] הדרושה לגוף מעולם לא נקבעה. הצהרה זו עדיין נכונה היום, יותר משבעים שנה אחרי זה."
בהמשך המאמר המחברים מחשבים את כמות היוד הדרושה לכל הגוף ע"י חישוב הכמות הדרושה לבלוטת התריס, והכמות הדרושה לשאר הגוף.
כמות היוד היומית הדרושה לבלוטת התריס
כדי לענות על שאלה זו החוקרים נעזרו בבדיקה של קליטת יוד רדיואקטיבי ע"י בלוטת התריס. עבור רמות שונות של צריכה יומית של יוד בדקו כמה יוד הבלוטה קלטה לאחר מתן מנה של יוד רדיואקטיבי. סיכום של המחקרים נמצא במאמר [27].
נמצא שברמות נמוכות של 20 מיקרוגרם הבלוטה קלטה כ 85% שזה 17 מיקרוגרם, וככל שהעלו את הרמה הבלוטה היתה יותר ויותר רוויה וקלטה פחות יוד רדיואקטיבי.
ברמה של 680 מיקרוגרם הקליטה היתה 15.4% (104 מיקרוגרם), וברמה של 10 mg כלומר 10,000 מיקרוגרם הקליטה היתה 4% (400 מיקרוגרם). כמות היוד הנקלטת ע"י בלוטת התריס מתייצבת על 600 מיקרוגרם ליום כאשר הצריכה היומית היא 6 mg ומעלה. מתוך המחקרים הללו ומחקרים נוספים שבחנו מתן תמיסת Lugol של יוד לחולי בלוטת התריס כותבי המאמר מגיעים למסקנה שהכמות האופטימלית עבור בלוטת התריס ליום היא תצרוכת יומית של 6 mg (לעומת 150 מיקרוגרם שקבע ה RDA - פי 40).
כמות היוד היומית הדרושה לשאר הגוף
מחקרים מראים שכאשר בלוטת התריס רוויה ביוד חלה ירידה במנגנון שקולט יוד בבלוטה, כלומר כדי לווסת את עצמה ולא לקלוט יותר מידי יוד יש מנגנון שיודע להוריד הילוך בקליטת היוד. זה קורה כאשר הצריכה היומית היא בסביבות 13 – 14 מ"ג ליום.
ראינו שהכמות היומית הדרושה לבלוטת התריס היא 6 מ"ג, מכאן לשאר הגוף דרוש כ 8 מ"ג, וחלק ניכר מהכמות הזו הולכת לרקמות בשד. כאמור יוד חשוב במניעה של סרטן שד, ולחומצות שומן מיודדות יש תפקיד בהגנה מפני סרטן, גם בשד וגם בבלוטת התריס, והן נוצרות כאשר רמת הצריכה היומית היא פי 100 מה- RDA.
במחקרים שנעשו על קליטת יוד ברקמות השונות של הגוף התגלה שבעוד שבלוטת התריס מעדיפה לקלוט יונים של יוד, רקמת השד מעדיפה לקלוט אטומים של יוד. על כן כאשר לוקחים תוסף של יוד חשוב שיהיה בו יוד בשתי הצורות הללו – כמו בתמיסת לוגול המקורית. הכמות המומלצת לשימוש בתמיסה הזו שהיתה נהוגה עד שנות ה 50 היא שתי טיפות, שמספק בדיוק 12.5 מ"ג של יוד.
בהנחה שחישבנו נכון את כמות היוד הדרושה לגוף ביום, העם היפני מהווה את האוכלוסיה היחידה בעולם שמגיעה לרמה הזו.
כיצד בודקים אם חסר לי יוד?
יש בדיקה פשוטה שניתן לעשות בבית, שיכולה לתת אינדיקציה אם חסר יוד בגוף. מורחים יוד על אזור של ארבע על ארבע סמ"ר, רצוי באזור לא חשוף כמו על הבטן, או בחלק האחורי של הברך. נותנים לזה להתיבש לפני שמכסים בבגד שכן היוד מכתים. בודקים במשך שתים עשרה שעות את הצבע של הכתם. אם הוא דוהה בפחות מ 12-14 שעות זה יכול להיות סימן שהגוף ספג את היוד וזו אינדיקציה שחסר יוד. פרטים נוספים על שיטה זו ניתן למצוא באתר של global healing.
שיטה זו קלה וזולה אולם אין שום מחקר מדעי שמאשש את מהימנותה. השיטה הטובה ביותר היא לבצע בדיקה של הפרשת היוד בשתן. זו הבדיקה שבה משתמשים כדי לאמוד את מצב היוד של אוכלוסיה, כאשר בודקים פרטים רבים ולוקחים את החציון. הבעיה עם הבדיקה הזו היא שכמות היוד המופרשת בשתן משתנה מאוד מיום ליום (עד פי שלוש), ואפילו לאורך שעות היום [28]. על כן בדיקת יוד בשתן בדגימה אחת לא יכולה לתת אינדיקציה קלינית לגבי מצב היוד של הנבדק.
ישנן שתי מעבדות שמציעות שרות של בדיקת יוד:
מעבדה בשם ZRT Laboratory מציעה בדיקה של שתן מיובש. טובלים סטריפ של ניר סופג בשתן ונותנים לו להתיבש. לבדיקה הזו נדרשות שתי דגימות מאותו היום. היתרון של הבדיקה הזו היא קלות האיסוף והמשלוח. החסרון של הבדיקה הזו הוא שלמעשה היא נותנת אינדיקציה לגבי כמות היוד בתזונה, אך היא אינה עוזרת לזהות מחסור ביוד.
מעבדה בשם Hakala Labs מציעה שתי בדיקות: בדיקה נקודתית ובדיקת העמסת יוד. בדיקה נקודתית בודקת את רמת השתן מדגימה אחת במשך היום והיא יעילה כדי לתת אינדיקציה למחסור חמור ביוד שעלול לגרום לגויטר (לפי המדד של ארגון הבריאות העולמי).
בדיקת העמסת יוד כרוכה בלקיחה של טבליה 50 מיליגרם של יוד, ולאחר מכן איסוף של כל השתן במשך 24 שעות. החסרון של הבדיקה הזו הוא שצריך לאסוף את כל השתן במשך 24 שעות ואם מפספסים פעם אחת זו בעיה. בנוסף גם המשלוח יותר מסובך. היתרון של בדיקה זו הוא שהיא נותנת אינדיקציה יותר מהימנה לגבי מצב היוד בגוף. אם יש בגוף כמות מספיקה, 90% מהיוד שלקחנו יופרש. אם מופרש פחות, זה סימן שחסר לגוף יוד. יש החוששים מלקיחת כמות כזו של יוד, אולם אצל רוב האנשים, כולל אלה שסובלים מהשימוטו, כמות חד פעמית אינה עושה בעיה. במקרים נדירים, אצל אנשים שסובלים מרעילות של ברום או פלואור עלול להופיע תסמיני דיטוקס מהחומרים הללו. מעבדת Hakala מאפשרת להוסיף בדיקה של חומרים אלה בשתן.
מה הקשר בין מצב היוד ורעילות של ברום ופלואור?
מבחינה כימית יוד שייך למשפחת ההלוגנים, שאליה משתייכים גם פלואור, כלור, וברום. מבין היסודות הללו, כלור ויוד דרושים לגוף ואילו פלואור וברום מזיקים לבריאות.
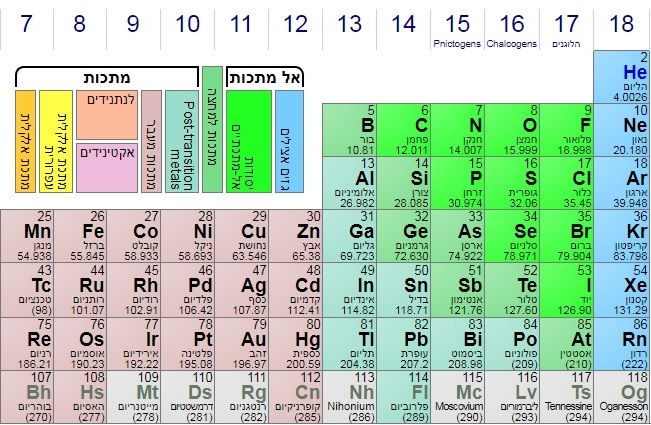
ברום הוא יסוד שמצוי בשפע בביוספרה, אולם עד עתה לא התגלה לו תפקיד חיוני בצמחים או בעלי חיים. להפך, מחקרים [29] מראים שברום מפריע למטבוליזם של יוד בגוף. ברום מגביר את ההפרשה של יוד בשתן ולכן אפילו אם אנו צורכים כמות מספיקה של יוד במזון, הוא מופרש והגוף לא יכול להשתמש בו. הברום גם מחליף את מקומו של היוד בבלוטת התריס וברקמת השד. בבלוטת התריס זה עלול לגרום לתת פעילות, על כן ברום מוכר כ"גויטרוגן". בשד הברום מחליף את היוד בחלב אם ולכן פוגע באספקה של יוד לתינוק היונק. האפקט המזיק של ברום מוגבר כאשר יש מחסור ביוד.
מאז שתעשיות הכימיה החלו להתפתח, ברום נכנס ליותר ויותר מוצרי צריכה. הברום מצוי בעיקר בחומרים מונעי בערה שמוסיפים אותם לכל מיני מוצרי צריכה כולל מזרנים ופיג'מות, בחומרי הדברה וכן במוצרי מזון וקוסמטיקה. יתכן מאוד שלחשיפה המוגברת של האוכלוסיה לברום יש חלק בעליה של ההיארעות של בעיות בבלוטת התריס.
רק לאחרונה [30], בשנת 2019, יזם הארגון האירופאי לבטיחות המזון מחקר שיבחן את ההשפעה המצטברת של חומרי הדברה במזון על מחלות של בלוטת התריס, וסרטן של בלוטת התריס בפרט.
פלואור אף הוא יסוד ממשפחת ההלוגנים, ולמרות המוניטין שהוא קיבל כמגונן על השיניים, מסתבר שהוא מזיק לתהליך של קליטת יוד בבלוטת התריס [31]. אנחנו חשופים לפלואור במשחות שינים ובמים מופלרים. פלואור מזיק גוף בעוד אופנים, ובאופן כללי אני ממליצה להפחית את החשיפה אליו.
אנחנו רואים שיש עוד גורמים שמשפיעים על המטבוליזם של יוד בגוף מעבר לרמת הצריכה של יוד. גם רמת החשיפה שלנו לברום ופלואור משפיעים ויכולים להזיק ולהחמיר מצב של מחסור ביוד.
מקורות של יוד בתזונה
יוד מצוי בעיקר במזונות שמקורם בים: אצות ים, דגים ופירות ים, והוא מצוי גם בכמות קטנה בקטניות.
באצות ים:
בכף של קלפ יש 2000 מיקרוגרם יוד
בכף של אראמה יש 730 מיקרוגרם יוד
בכף של היזיקי יש 780 מיקרוגרם יוד
בכף של קומבו יש 1450 מיקרוגרם יוד
בכף של ווקמה יש 80 מיקרוגרם יוד
בכף של פתיתי דולס מיובשים יש 852 מיקרוגרם יוד
לשם השוואה, בכוס אפונה ירוקה מבושלת יש רק 6 מיקרוגרם יוד.
סיכום טענות המצדדים בהגברה של הצריכה של יוד
יוד היה בשימוש נרחב כטיפול לכל מיני בעיות בריאות מסוף המאה ה 19 במינון פי מאה מהמינון המוגדר היום כעודף של יוד, ללא כל תופעות חריגות או התפתחות של מחלות אוטואימוניות בבלוטה. יוד דרוש להרבה רקמות בגוף, לא רק לבלוטת התריס, ובפרט הוא חשוב לבריאות השדיים. תהליכי המטבוליזם של יוד בגוף כרוכים באוסף של חומרים כמו סלניום, מגנזיום, ברום ופלואור. מחסור בחומרים הדרושים או חשיפה מוגברת לברום ופלואור עשויים להסביר את ההתגברות של המחלות האוטואימוניות בבלוטת התריס.
נסיון של עבודה עם מטופלים מראה שכאשר בדיקת העמסת יוד מראה חוסר ביוד, לוקח 3-6 חודשים של מתן תוסף יוד עד להגעה לרוויה ובמקביל רואים שיפור במצב הבריאותי של המטופל.
המסקנות שלי לגבי יוד
שאלה שעלתה לי תוך כדי הכנת המאמר הזה היא השאלה האבולוציונית. בני אדם התפתחו על פני כדור הארץ עם כמות היוד המצויה בו, ושכנו לא רק ליד חופי הים. כיצד יתכן שהתפתחנו להצטרך יותר יוד ממה שיש לקרקע להציע לנו? או שמה שקרה זה שהתזונה שלנו השתנתה מאוד ממה שאכלו אבותינו הציידים-לקטים, ושיטות החקלאות המודרניות שאבו מן האדמה את מלאי היוד שהיה בה והפכו את האדמה החקלאית שלנו לענייה ביוד?
בכל מקרה, מכל הדיון הזה אני לוקחת כמה תובנות:
חשוב להיות במודעות לגבי כמות היוד שאני צורכת.
אין המלצה גורפת שנכונה לכולם, כל אחד הוא אינדיבידואל וצריך לבחון את המקרה שלו לגופו.
לפני שעושים שינוי בתזונה (הוספה או הפחתה של צריכת היוד) כדאי לעשות בדיקת העמסת יוד כדי לבחון מה המצב.
אם הבדיקה מראה שחסר יוד כדאי לנסות להעלות את צריכת היוד בהדרגה עד לרמה של 12.5 מ"ג ליום (שילוב של iodine ו- iodide) ולאחר שלושה חודשים עד חצי שנה לעשות בדיקת העמסת יוד להערכת המצב מחדש. כמו כן להיות במעקב אחר רמת הנוגדנים.
כדאי לבדוק גם את מצב הברום והפלואור ולהפחית את החשיפה אליהם.
אם רמת הנוגדנים גבוהה בתפריט ללא גלוטן, שווה לנסות להוסיף סלניום, חומצה אלפא ליפואית ו N אצטיל סיסטאין (NAC) כדי להעלות את רמת הגלותתיון ולבדוק אם יש שינוי לטובה. אפשר גם לבדוק תזונה מופחתת יוד ולראות אם יש שינוי לטובה.
כשמבינים את מקור הבעיה זה הצעד הראשון לריפוי.
מוזמנים ליצור קשר עימי להתיעצות לגבי האתגר שלכם. יעל שחם גפני
מקורות
Iodine Status Worldwide, WHO Global Database on Iodine Deficiency, 2003
Urinary Iodine Concentrations for Determining Iodine Status in Populations. World Health Organization. 2013.
Ahad, Farhana, and Shaiq A Ganie., Iodine, Iodine metabolism and Iodine deficiency disorders revisited. Indian journal of endocrinology and metabolism vol. 14,1 (2010): 13-7.
https://www.thyroidmanager.org/chapter/chapter-2-thyroid-hormone-synthesis-and-secretion/
Teti C, Panciroli M, Nazzari E, Pesce G, Mariotti S, Olivieri A, Bagnasco M. Iodoprophylaxis and thyroid autoimmunity: an update. Immunol Res. 2021 Apr;69(2):129-138. doi: 10.1007/s12026-021-09192-6. Epub 2021 Apr 29. PMID: 33914231.
Zhao W, Han C, Shi X, Xiong C, Sun J, Shan Z, Teng W. Prevalence of goiter and thyroid nodules before and after implementation of the universal salt iodization program in mainland China from 1985 to 2014: a systematic review and meta-analysis. PLoS One. 2014 Oct 14;9(10):e109549. doi: 10.1371/journal.pone.0109549. PMID: 25313993; PMCID: PMC4196906.
Kochupillai N, Mehta M. Iodine deficiency disorders and their prevention in India. Rev Endocr Metab Disord. 2008 Sep;9(3):237-44. doi: 10.1007/s11154-008-9094-0. PMID: 18663580.
Delange FM. Control of iodine deficiency in Western and Central Europe. Cent Eur J Public Health. 2003 Sep;11(3):120-3. PMID: 14514161.
Ovadia YS, Arbelle JE, Gefel D, Brik H, Wolf T, Nadler V, Hunziker S, Zimmermann MB, Troen AM. First Israeli National Iodine Survey Demonstrates Iodine Deficiency Among School-Aged Children and Pregnant Women. Thyroid. 2017 Aug;27(8):1083-1091. doi: 10.1089/thy.2017.0251. PMID: 28657479.
Heydarian P, Ordookhani A, Azizi F. Goiter rate, serum thyrotropin, thyroid autoantibodies and urinary iodine concentration in Tehranian adults before and after national salt iodization. J Endocrinol Invest. 2007 May;30(5):404-10. doi: 10.1007/BF03346318. PMID: 17598973.
Azizi F, Navai L, Fattahi F. Goiter prevalence, urinary iodine excretion, thyroid function and anti-thyroid function and anti-thyroid antibodies after 12 years of salt iodization in Shahriar, Iran. Int J Vitam Nutr Res. 2002 Oct;72(5):291-5. doi: 10.1024/0300-9831.72.5.291. PMID: 12463103.
Zaletel K, Gaberscek S, Pirnat E. Ten-year follow-up of thyroid epidemiology in Slovenia after increase in salt iodization. Croat Med J. 2011 Oct 15;52(5):615-21. doi: 10.3325/cmj.2011.52.615. PMID: 21990079; PMCID: PMC3195970.
Latrofa F, Fiore E, Rago T, Antonangeli L, Montanelli L, Ricci D, Provenzale MA, Scutari M, Frigeri M, Tonacchera M, Vitti P. Iodine contributes to thyroid autoimmunity in humans by unmasking a cryptic epitope on thyroglobulin. J Clin Endocrinol Metab. 2013 Nov;98(11):E1768-74. doi: 10.1210/jc.2013-2912. Epub 2013 Sep 24. PMID: 24064687.
Kahaly G, Dienes HP, Beyer J, Hommel G. Randomized, Double Blind, Placebo-Controlled Trial of Low Dose Iodide in Endemic Goiter. J Clin Endocrinol Metab. 1997;82(12):4049-4053. doi:10.1210/jcem.82.12.4416.
Rink T, Schroth H, Holle L, Garth H. Effect of iodine and thyroid hormones in the induction and therapy of Hashimoto’s thyroiditis. Nuklearmedizin. 2016;1999(38(5):144-9.
Mario Vitale, Tiziana Di Matola, Francesca D’Ascoli, Salvatore Salzano, Fausto Bogazzi, Gianfranco Fenzi, Enio Martino, Guido Rossi, Iodide Excess Induces Apoptosis in Thyroid Cells through a p53-Independent Mechanism Involving Oxidative Stress, Endocrinology, Volume 141, Issue 2, February 2000, Pages 598–605
Kolypetri P, Carayanniotis G. Apoptosis of NOD.H2 h4 thyrocytes by low concentrations of iodide is associated with impaired control of oxidative stress. Thyroid. 2014 Jul;24(7):1170-8. doi: 10.1089/thy.2013.0676. Epub 2014 May 28. PMID: 24660772; PMCID: PMC4080865.
Xue H, Wang W, Li Y, Shan Z, Li Y, Teng X, Gao Y, Fan C, Teng W. Selenium upregulates CD4(+)CD25(+) regulatory T cells in iodine-induced autoimmune thyroiditis model of NOD.H-2(h4) mice. Endocr J. 2010;57(7):595-601. doi: 10.1507/endocrj.k10e-063. Epub 2010 Apr 27. PMID: 20453397.
Joung JY, Cho YY, Park SM, Kim TH, Kim NK, Sohn SY, Kim SW, Chung JH. Effect of iodine restriction on thyroid function in subclinical hypothyroid patients in an iodine-replete area: a long period observation in a large-scale cohort. Thyroid. 2014 Sep;24(9):1361-8. doi: 10.1089/thy.2014.0046. Epub 2014 Jun 30. PMID: 24892764.
Kasagi K, Iwata M, Misaki T, Konishi J. Effect of iodine restriction on thyroid function in patients with primary hypothyroidism. Thyroid. 2003 Jun;13(6):561-7. doi: 10.1089/105072503322238827. PMID: 12930600.
Yoon SJ, Choi SR, Kim DM, Kim JU, Kim KW, Ahn CW, Cha BS, Lim SK, Kim KR, Lee HC, Huh KB. The effect of iodine restriction on thyroid function in patients with hypothyroidism due to Hashimoto's thyroiditis. Yonsei Med J. 2003 Apr 30;44(2):227-35. doi: 10.3349/ymj.2003.44.2.227. PMID: 12728462.
Abraham, G.E, MD., The History of Iodine in Medicine Part I: From Discovery to Essentiality. The Original Internist, 13: 29-36, Spring 2006
Abraham, G.E., The History of Iodine in Medicine Part II: The Search for and the Discovery of Thyroid Hormones, The Original Internist, 13: 67-70, June 2006
Abraham, G.E., The History of Iodine in Medicine Part III: Thyroid Fixation and Medical Iodophobia. The Original Internist, 13: 71-78, June 2006
Eskin BA., Iodine and Mammary Cancer, Tans NY, Academy of Sciences 1970.
Zava TT, Zava DT. Assessment of Japanese iodine intake based on seaweed consumption in Japan: A literature-based analysis. Thyroid Res. 2011;4:14. Published 2011 Oct 5. doi:10.1186/1756-6614-4-14
Abraham, G.E., Flechas, J.D., Hakala, J.C. Iodine sufficiency of the whole human body., The Original Internist 9: 30-41, 2002.
Rasmussen LB, Ovesen L, Christiansen E. Day-to-day and within-day variation in urinary iodine excretion. Eur J Clin Nutr. 1999 May;53(5):401-7. doi: 10.1038/sj.ejcn.1600762. PMID: 10369497.
Pavelka S. Metabolism of bromide and its interference with the metabolism of iodine. Physiol Res. 2004;53 Suppl 1:S81-90. PMID: 15119938.
European Food Safety Authority (EFSA), Crivellente F, Hart A, Hernandez-Jerez AF, Hougaard Bennekou S, Pedersen R, Terron A, Wolterink G, Mohimont L. Establishment of cumulative assessment groups of pesticides for their effects on the thyroid. EFSA J. 2019 Sep 17;17(9):e05801. doi: 10.2903/j.efsa.2019.5801. PMID: 32626429; PMCID: PMC7009157.
Waugh DT. Fluoride Exposure Induces Inhibition of Sodium/Iodide Symporter (NIS) Contributing to Impaired Iodine Absorption and Iodine Deficiency: Molecular Mechanisms of Inhibition and Implications for Public Health. Int J Environ Res Public Health. 2019 Mar 26;16(6):1086. doi: 10.3390/ijerph16061086. PMID: 30917615; PMCID: PMC6466022.


תגובות